Ce fameux gluten. Difficile de passer à côté des débats médiatiques relatifs à cette protéine issue de certaines céréales, notamment du blé, et qui serait à l’origine de nombreux maux de la société moderne, depuis la simple fatigue jusqu’aux pathologies auto-immunes. Mais, qu’en est-il précisément ?
Il est difficile de répondre à cette question. Les connaissances évoluent en effet en permanence (les miennes y compris) et se retrouvent au cœur de débats scientifiques. Certains considèrent qu’en dehors de la maladie cœliaque, la problématique du gluten est inexistante voire un faux problème. Pour d’autres, cette protéine serait à bannir totalement au regard des conséquences multiples, pour ne pas dire dramatiques, sur la santé. Bien sûr, le premier camp juge le second comme incompétent et dogmatique, tandis que le second considère le premier totalement fermé à toute actualisation de ses connaissances. Je vous propose de tenter d’y voir plus clair.
Si vous souhaitez aller à l’essentiel
Qu’est-ce que le gluten ?
Vous l’avez sans doute déjà lu, gluten vient de « glu » signifiant colle. Il s’agit de la réserve protéique nécessaire à la germination du grain. Plus précisément, le gluten est la fraction insoluble des protéines, elle-même constituée de deux sous-unités : les prolamines et les glutélines (dans le cas du blé, la céréale aujourd’hui au cœur du sujet, il s’agit respectivement des gliadines et des gluténines). La fraction protéique incriminée dans la maladie cœliaque et les hypersensibilités au gluten fait partie de la famille des prolamines, présente sous différentes formes selon les céréales : alpha-gliadine dans le cas du blé, sécaline dans le cas du seigle et hordénine dans le cas de l’orge (le maïs contient de la zénine pouvant également générer une réaction).
L’avoine est un cas plus spécifique. Issu de la famille des avénées, il contient de l’avénine, dont les effets peuvent être différents en fonction de la variété7,8. Chez les malades cœliaques, la variété Nave semble entraîner une réponse immunitaire, à la différence des variétés Potenza et Irina. Prudence donc, d’autant qu’il peut exister des contaminations croisées avec des céréales contenant du gluten sur les chaines de production.
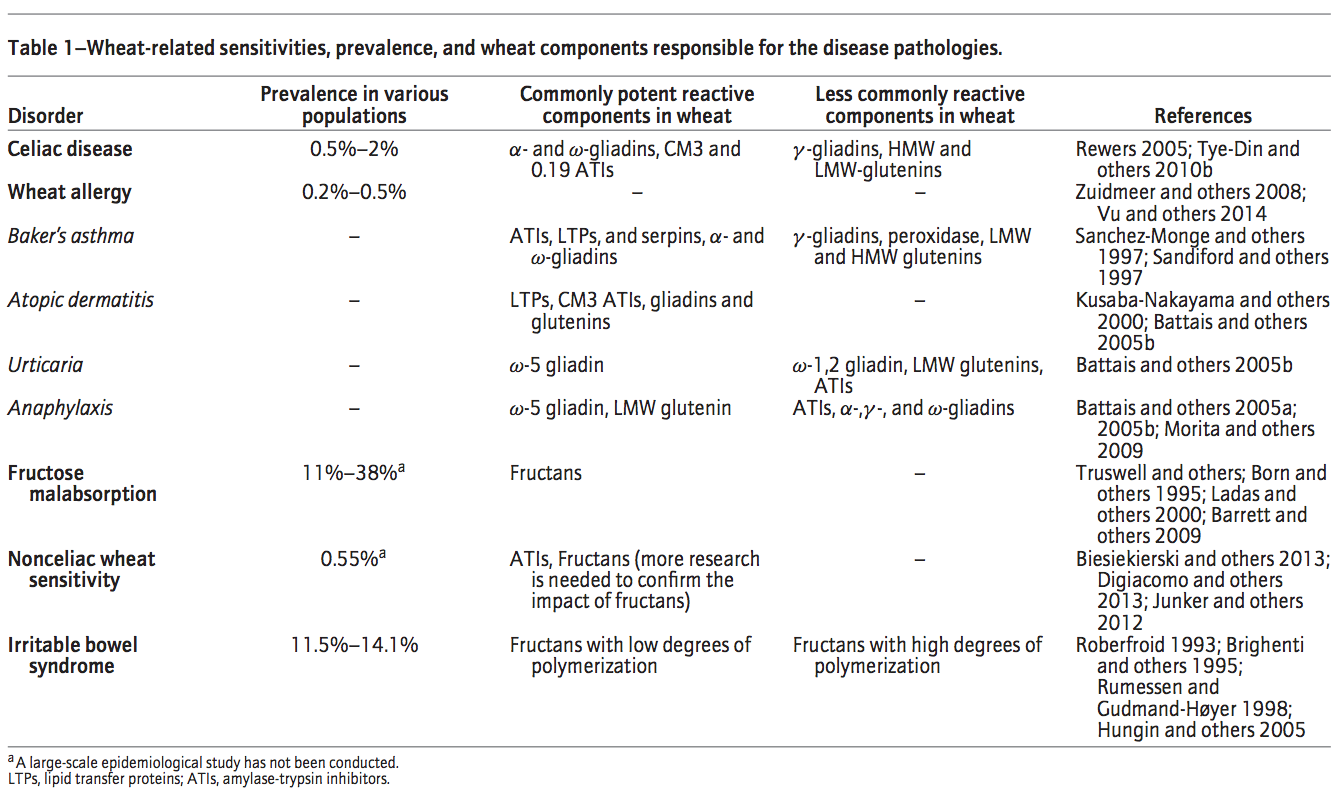
Source : Comprehensive Reviews in Food Science and Food Safety Vol. 14, 2015
Une des spécificités du gluten, et en particulier de la gliadine du blé, est d’être constitué de peptides riches en acides aminés, la proline et la glutamine, capables de résister aux enzymes digestives (les protéases). L’arrivée de la gliadine dans l’intestin fait alors l’objet d’une réaction immunitaire chez certains individus. Pour autant, il existe de nombreux aliments pouvant déclencher une telle réponse, alors pourquoi le gluten génère-t-il autant d’attention ? Avant tout car il est omniprésent dans l’alimentation moderne, en particulier lorsque celle-ci est transformée. Le gluten possède en effet la propriété inégalée de conférer à la pâte formée par un mélange d’eau et de farine de l’élasticité, de la cohésion et de la force. Dans le cas du pain ou des aliments utilisant de la levure ou du levain, le gluten hydraté au cours du pétrissage permet de retenir les gaz issus de la fermentation pour créer une belle boule de pâte aérée qui donnera naissance, une fois cuite, à un appétissant pain alvéolé et moelleux à souhait. Les hommes l’ont bien compris depuis des milliers d’années.
La culture du blé est apparue il y a environ 10 000 ans entre la Mésopotamie et l’Égypte et le pain occupe depuis une place centrale dans l’alimentation des populations, y compris au sens symbolique. Depuis l’essor de l’industrie agro-alimentaire, les recherches visant à accroitre cette propriété naturelle du blé se sont concentrées sur la façon d’augmenter le taux et la force du gluten dans les farines. Les semenciers ont de leur côté cherché à obtenir des épis de blé plus courts, donc plus faciles à récolter et plus résistants aux maladies, ce toujours dans une optique de rendement. Il existe plusieurs façons de sélectionner les meilleurs blés : depuis le choix d’épis s’égrenant peu (sélection initiale) et de grains issus des plus beaux épis pour la culture de l’année suivante (sélection massale) en passant par la délocalisation de la culture hors du milieu d’origine vers un environnement plus propice mais aussi, et surtout pour ce qui concerne le blé, par l’hybridation. Celle-ci consiste à croiser des espèces entre-elles pour obtenir des plants plus productifs. Une telle méthode est souvent confondue avec la modification génétique (les célèbres OGM), ce qui est radicalement différent. Par l’hybridation, l’homme est à l’origine d’une forte évolution phylogénique du blé. Un de ses premiers ancêtre fortement cultivé fut le Triticum monococcum, également connu sous le nom de petit épeautre. Il possède 7 paires de chromosomes. Son hybridation avec l’herbe folle, Aegylops speltoïdes, également composé de 7 paires de chromosomes, a donné naissance à une forme diploïde et, dans des rares cas, à une forme tétraploïde à 14 paires de chromosomes. Par la suite, de nombreuses recombinaisons et mutations ont permis l’apparition de Triticum dicoccum puis de Triticum durum, une variété de blé dur constitué de 14 paires de chromosomes. De cette hybridation est née le kamut. Triticum dococcum a par la suite été hybridé avec Aegylops squarrosa, donnant naissance à l’ancêtre de Triticum Aestivum, plus connu sous le nom de… blé tendre ou de froment, à savoir le blé le plus consommé actuellement. Il s’agit d’une forme hexaploïde composée de 21 paires de chromosomes, bien différente de la forme ancestrale du blé. L’orge et le seigle possèdent quant à eux 7 paires de chromosomes mais sont également diploïdes, ce qui laisse suggérer qu’ils possèdent un ancêtre commun au blé. De manière simplifiée, on peut considérer que le blé est génétiquement très proche de l’orge, un peu moins du seigle et encore un peu moins de l’avoine. A l’inverse le riz, le maïs et les céréales africaines (millet, sorgho, fonio) en sont dénués et sont génétiquement très éloignés du blé.
L’obtention d’un tel blé est une manne pour l’industrie agro-alimentaire. L’utilisation de sa farine permet en effet d’améliorer de nombreuses étapes de panification, notamment en remplaçant le levain traditionnel par de la levure. Les grains utilisés ne sont par ailleurs pas germés, la farine raffinée (blanche) permet d’accroitre encore davantage le taux de gluten et de faciliter le travail de la pâte, la vitesse de pétrissage est plus rapide, les taux d’hydratation et d’acidité sont adaptés, le temps de levée est raccourci et la cuisson peut être portée à plus haute température. Tout a été réuni pour obtenir un pain plus aéré, plus moelleux et pour gagner du temps, donc de l’argent. Mais, comme si ce n’était pas suffisant, du gluten pur est rajouté dans les farines panifiables (sans parler des autres additifs) afin d’accentuer encore ce bénéfice. C’est également le cas dans un grand nombre de produits industriels, à l’image du surimi et des produits reconstitués à base de viande. Se pose donc la question des conséquences potentielles de tels changements sur la santé.
Deux points sont importants à considérer : les effets du niveau d’exposition au gluten augmentant fortement dans un contexte d’écosystème intestinal perturbé par d’autres facteurs d’une part et, d’autre part, la capacité de l’organisme à tolérer un gluten rendu plus fort mais aussi les auxiliaires technologiques utilisés, comme la transglutaminase dont nous reparlerons.
Il existe plusieurs troubles consécutifs à l’exposition au gluten : la maladie cœliaque, la dermatite herpétiforme, l’allergie au blé et l’hypersensibilité non cœliaque12.
Faut-il éviter le gluten ?
La réponse à cette question dépendra de votre situation. Je vous précise par ailleurs ici la partie pratique de l’article, davantage d’explications vous sont détaillées dans la seconde partie.
1. Vous souffrez de maladie cœliaque, d’ataxie au gluten, de dermatite herpétiforme ou d’allergie au blé
La maladie coeliaque concerne est une maladie pouvant être considérée de type auto-immun, se traduisant par des diarrhées, une malabsorption intestinale des nutriments et toutes les conséquences que celle-ci engendre à long terme (perte de poids, fatigue, carences diverses, etc.).
L’ataxie au gluten est une maladie également de type auto-immune, mais atteignant le système neurologique.
La dermatite herpétiforme est la maladie cœliaque touchant la peau. Elle se traduit par l’apparition de petites vésicules cutanées associées à de fortes démangeaisons.
L’allergie au blé est comme son nom l’indique, une allergie et non une atteinte des villosités intestinales comme dans le cas de la maladie cœliaque.
Dans ces situations, la question ne se pose pas. Il est indispensable de supprimer toute source de gluten (ou de blé dans le cas de l’allergie au blé). A mon sens, l’éviction de l’avoine, y compris lorsque la variété est mentionnée sans gluten, se justifie dans la plupart des cas. Les pommes de terre et le maïs peuvent également être à supprimer chez certaines personnes. Par ailleurs, si vous souffrez des signes évoqués dans la partie développée à la fin de l’article, je vous conseille d’en parler à un médecin sensible au sujet pour analyser l’intérêt de réaliser un dosage sanguin, voire une biopsie villositaire. Une étude canadienne a par exemple mis en évidence qu’une démarche médicale active de recherche en ce sens permettait de multiplier par 32 à 44 le taux de diagnostic de maladie cœliaque.
Le simple dosage sanguin de recherche d’anticorps ne suffit par ailleurs pas à éliminer l’existence de cette maladie, la biopsie non plus si vous avez déjà arrêté le gluten depuis plusieurs semaines au moment où vous réalisez l’examen.
Plus de 80% des malades cœliaques s’ignorent…
2. Vous pensez souffrir d’une intolérance aux fructanes (FODMAP)
Il s’agit d’une intolérance à certaines fibres fermentescibles, les fructanes, abondantes dans les céréales contenant du gluten. Elles sont souvent considérées comme les responsables des troubles digestifs dont se plaignent les personnes s’estimant hypersensibles au gluten : diarrhées, ballonnements, gaz, etc.
Dans cette situation, la démarche est radicale mais relativement simple (dans le principe) : il est nécessaire de supprimer tous les aliments contenant des FODMAP pendant quelques semaines. Si vous êtes concerné(e), je vous recommande de réaliser ce régime avec l’aide de votre professionnel de santé et en complément d’une action globale sur la restauration de votre écosystème intestinal (muqueuse et microbiote). Dans le cadre de mes suivis individuels et en cas de doute, après avoir réalisé l’éviction totale des FODMAP dans un premier temps, je fonctionne par la suite en deux étapes. Je rétablis d’abord progressivement l’ensemble des aliments contenant des FODMAP en complément d’un travail sur l’écosystème intestinal, sauf ceux contenant des fructanes (dont le seigle, le blé et l’orge). Puis je propose de les réintroduire dans un second temps. Si les symptômes reviennent, l’éviction est nécessaire, qu’il s’agisse d’une intolérance aux fructanes ou d’une hypersensibilité au gluten.
Par ailleurs, si vous souffrez de symptômes extra-digestifs (inflammations chroniques et troubles immunitaires notamment), il est probable que vous soyez davantage concerné(e) par une hypersensibilité au gluten que par une intolérance aux fructanes.
Aliments contenant des FODMAP
Supprimer pendant au moins cinq semaines les aliments contenant du gluten, à savoir les aliments contenant du froment, du seigle, de l’orge et la plupart des variétés d’avoine contenant ces céréales (biscuits, pâtisseries, pâtes, pain, farine, etc.).
Il est également important de bien lire les étiquettes de produits industriels si vous en consommez, pour vérifier notamment l’absence des mentions « blé, seigle, orge, avoine (si non garanti sans gluten), amidon, matières amylacées, protéines végétales (si l’origine n’est pas précisée) ». Privilégier les produits céréaliers (ou aliments contenant de l’amidon) sans gluten : riz, quinoa, sarrasin, châtaigne, soja, patate douce, tapioca, légumineuses si vous les tolérez au niveau intestinal. Il existe aujourd’hui de nombreux produits sans gluten, dont certains pains de bonne qualité réalisés au levain traditionnel par votre artisan-boulanger.
Les produits soufflés (crackers de sarrasin, galettes de riz ou de maïs, etc.) possèdent un index glycémique élevé, privilégier donc les produits bruts. Les variétés d’avoine garanties sans gluten (notamment du müesli) sont identifiables grâce au logo mentionnant un épi de blé barré sur l’emballage.
Attention aux produits industriels sans gluten utilisant des additifs en substitution du gluten, à éviter (pain de mie, biscuits, etc.) au profit des produits bruts. Après les cinq premières semaines et si vous ne souffrez pas de maladie cœliaque (ou ataxie au gluten ou dermatite herpétiforme), d’allergie au blé ou d’intolérance aux fructanes, le petit épeautre peut représenter une alternative au blé moderne intéressant s’il est consommé avec modération sous forme notamment de farine ou de pain au pur levain à fermentation longue. De nombreux magasins en proposent désormais.
3. Vous pensez souffrir d’hypersensibilité non cœliaque au gluten
L’hypersensibilité non cœliaque au gluten ou NHGS (pour non-cœliac gluten sensibility), communément appelée (à tort) intolérance au gluten est au cœur du sujet. Il s’agit d’une réaction exacerbée de votre organisme suite à la consommation de gluten, différente de la maladie cœliaque, pouvant se traduire par des symptômes non spécifiques et selon un niveau de tolérance variable. Certaines personnes pourront très bien tolérer une quantité modérée (en consommant par exemple du petit épeautre au lieu du blé) alors que d’autres seront proches d’une situation cœliaque. Selon les études récentes, jusqu’à 13% de la population française serait touchée.
L’hypersensibilité non cœliaque au gluten peut se manifester par les symptômes suivants (non exhaustifs et non spécifiques) : douleurs abdominales, brûlures épigastriques, rétention d’eau, nausées, diarrhées, constipation, maux de tête, fatigue chronique, troubles immunitaires (susceptibilités aux infections, allergies, hypersensibilités à d’autres aliments ou composés non alimentaires, pathologies auto-immunes), troubles inflammatoires (troubles en -ite, en particulier au niveau ostéo-articulaires ou des microcapillaires), voire troubles du comportement (autisme, troubles de l’attention avec ou sans hyperactivité).
Si vous vous sentez concerné(e), il existe une solution simple : faites le test de supprimer toute source de gluten pendant cinq semaines (voir encadré), mais faites-le totalement. La présence de gliadines, même en petites quantités, peut en effet suffire à biaiser les résultats de votre test. L’hypersensibilité n’est en effet pas obligatoirement liée à la quantité de gluten consommée mais à votre réactivité à cette protéine. Au terme de cette période, faites un bilan :
- Si les symptômes pour lesquels vous avez arrêté le gluten s’améliorent ou ont disparu. Vous êtes sur la bonne voie. Poursuivez ainsi, il n’y a aucun risque de déséquilibre nutritionnel contrairement à ce que prétendent certains professionnels ou médias. Pour assurer un bon équilibre de votre alimentation, je vous recommande toutefois d’être accompagné(e) par un professionnel compétent sur le sujet, il vous guidera de façon à prendre soin de vous grâce à une nutrition adaptée.
- Si les symptômes ne se sont pas améliorés. Je vous recommande là aussi de vous rapprocher d’un professionnel de santé pour personnaliser votre démarche car de nombreuses raisons peuvent expliquer une telle situation : maintien involontaire de gluten, durée d’éviction trop courte, réaction inadaptée à d’autres peptides alimentaires que le gluten (caséines ou bêta-lactoglobulines du lait, œufs, etc.) et/ou à d’autres composés (sulfites notamment), absence de restauration de l’écosystème intestinal (maintien de l’hyperperméabilité, manque de mastication, traitement médicamenteux, stress, consommation d’alcool, manque de fibres, pratique sportive intensive, absence de prise de probiotiques de qualité, maintien de perturbateurs intestinaux comme le bisphénol A ou les édulcorants, etc.). En effet, je vous invite d’ailleurs à découvrir la partie développée de l’article à ce sujet, une perméabilité importante de la muqueuse intestinale explique en grande partie l’apparition des symptômes liées à l’hypersensibilité au gluten.
Manger sans gluten présente-t-il un risque pour la santé ?
Les arguments des détracteurs d’une alimentation pauvre en gluten sont nombreux : déficits énergétiques, augmentation des risques de diabète, de maladies cardio-vasculaires (1, 2, 3) ou de contamination à l’arsenic, etc. Ils sont pourtant totalement subjectifs pour deux raisons principales. D’une part les études réalisées sont souvent biaisées dans la mesure où les aliments remplaçant ceux sans gluten sont des produits industrialisés. D’autre part, les personnes recrutées dans l’étude ne disposent pas de conseils suffisants pour savoir comment équilibrer leur alimentation face à ce nouveau modèle alimentaire et les études se base sur des recueil de données (fondées sur le souvenir des participants). Le gluten ne présente en effet aucune spécificité devant laisser craindre une carence, dès lors que vous portez vos choix alimentaires de façon à équilibrer vos besoins quotidiens, à varier les aliments et que vous ne vous tournez pas le dos du gluten au profit de produits industrialisés bourrés (je me permets) d’additifs palliant l’intérêt technologique du gluten. Je l’évoque régulièrement dans mes articles, comme par exemple dans celui relatif à l’arsenic et au régime sans gluten.
Dans tous les cas, que vous soyez ou non hypersensibles au gluten
Je vous conseille de réduire votre consommation de gluten si vous êtes un fort consommateur de produits à base de blé (pain, pâtes, farines, biscuits, plats industriels en contenant, etc.), pour différentes raisons. D’une part l’alimentation moderne conventionnelle est beaucoup trop insulino-secrétrice. Par ailleurs, les facteurs environnementaux d’altération de l’écosystème intestinal sont tels que la probabilité de déclencher une réponse inadaptée à certains peptides alimentaires au cours du temps est de plus en plus forte dans notre société actuelle. Par ailleurs, la consommation de gluten présente cette particularité d’être une cause potentielle d’altération de votre écosystème intestinal, au-delà d’une conséquence des symptômes de l’hypersensibilité.
Il existe tant de légumineuses, de tubercules et de produits céréaliers complets bio à l’index glycémique plus faible, plus riches en micronutriments ou encore en fibres, qu’il serait bien dommage d’accorder une place de choix au blé…
Si vous souhaitez malgré tout conserver de grandes quantités de produits céréaliers à base de blé « classique » , je vous conseille alors de vous orienter vers des aliments à base d’épeautre voire d’engrain.
Si vous aimez le pain et que vous le tolérez, privilégiez un pain au pur levain, bio, à fermentation longue, de préférence au petit épeautre ou au seigle complet, fabriqué par un artisan amoureux de son métier, mieux encore, par un paysan-boulanger cultivant ses propres variétés à partir de semences anciennes. Une étude récente a d’ailleurs mis en évidence que l’origine géographique est tout aussi importante que le caractère ancien du blé (4).
Le pain au pur levain à fermentation longue, la solution ?
Une des autres hypothèses émises pour expliquer les désordres liés à la consommation de gluten serait l’utilisation abondante de levure dans les pains et le raccourcissement de la durée de fermentation. Le levain contient en effet des enzymes actives, les protéases, favorisant la fragmentation (l’hydrolyse) du gluten et donc sa tolérance, notamment grâce à une meilleure efficacité des enzymes pancréatiques et à une hydratation importante de la pâte, nécessaire à la dénaturation des protéines.
Il ne s’agit donc nullement de tomber dans quelque dogmatisme que ce soit – dans un sens ou un autre d’ailleurs – mais simplement :
- De faire preuve avant tout de bon sens, en privilégiant une alimentation brute, issue de végétaux les plus anciens possibles, que vous prenez plaisir à cuisiner.
- De placer le curseur de votre exposition au gluten en fonction de votre situation personnelle, idéalement avec l’aide d’un professionnel de la santé formé à la nutrition.
Mais surtout, ne vous faites pas avoir par les sirènes du marketing des produits ultra-transformés, vous proposant nombre de cochonneries très chères au nom d’un logo « gluten-free ».
La recherche de rendements industriels au cœur du problème
Vous le savez peut-être déjà et sans doute si vous avez déjà tenté de faire vous-même du pain sans gluten, le gluten est allègrement utilisé par l’industrie de la panification et céréalière pour ses propriétés viscoélastiques. Il confère en effet à la pâte à pain ses capacités d’élasticité et de rétention des gaz produits sous l’effet de la fermentation. Une présence importante de gluten permet ainsi d’utiliser des grains non germés et des farines raffinées (à notre grand damne nutritionnel !), de réduire le temps de fermentation à la levure, de pétrissage à des vitesses rapides ou encore d’augmenter la température de cuisson. Il en est de même pour l’agriculture. La sélection et l’hybridation de blés plus résistants aux maladies, plus faciles à découper et à récolter, concentrant jusqu’à deux fois la quantité de gluten dans le blé dit « moderne », dur ou tendre (Triticum turgidum subsp. Durum et Triticum aestivum) en comparaison d’une forme ancienne comme l’engrain (Triticum monococcum), sans compter sur son rajout en tant qu’additif dans de nombreuses farines et autres produits amidonnés industriels (pâtisseries, viennoiseries, etc.). C’est ainsi que le niveau d’exposition au gluten a littéralement explosé au cours des dernières décennies et, qu’associé aux nombreux facteurs à l’origine d’une hyperperméabilité intestinale, il en résulte un cocktail idéal pour augmenter les réponses inadaptées au gluten, au moins quatre fois plus fréquentes qu’il y a 50 ans (5). Petite digression du sujet. Cette sélection de variétés explique non seulement les modifications de teneur en gluten, mais aussi en fibres et en antioxydants (6).
Nutritionnellement
Anthony Berthou
Si vous souhaitez comprendre plus en détails les différentes raisons pouvant expliquer une difficulté à tolérer le gluten
Les différents types de réaction au gluten
Quelques rappels de sémantique sont nécessaires avant d’aborder le sujet en détail. Il existe en effet de nombreuses situations pouvant expliquer une réaction inadaptée à la suite de la consommation de gluten.
1. La maladie coeliaque
La maladie cœliaque toucherait moins de 1% de la population13,14. Aux États-Unis, 0,3 à 0,4% de la population serait cœliaque sans le savoir, soit 30 à 40% des personnes touchées16. Il s’agit d’une maladie pouvant être considérée de type auto-immun, se traduisant par des diarrhées, une malabsorption des nutriments et toutes les conséquences que celle-ci engendre à long terme (perte de poids, fatigue, carences, ostéoporose, etc.). Il existe une part de prédisposition génétique dans cette maladie.
La maladie coeliaque est diagnostiquée par la recherche d’immunoglobulines de type IgA ou IgG d’une part et grâce à une biopsie intestinale d’autre part. Cette dernière révèle notamment une altération de l’intégrité de la muqueuse (ce que l’on nomme une atrophie villositaire) expliquant l’apparition des carences en nutriments. On estime pour autant que seule 10 à 20% de la population cœliaque serait diagnostiquée, ce qui pourrait apporter une explication à toute une partie de la population souffrant des symptômes évoqués et se questionnant sur l’origine exacte.
A noter que l’interprétation de la biopsie doit être effectuée par un expert pathologiste. Il existe en effet de nombreux faux-négatifs, à savoir que le test apparaît de prime abord négatif alors que la pathologie existe bel et bien. Par ailleurs, une analyse effectuée auprès d’enfants de moins de 2 ans est peu fiable. De même, les résultats peuvent être biaisés lorsque la personne a déjà mis en place un régime pauvre ou sans gluten, en cas de déficit sélectif en IgA, de prise de corticoïdes ou de modulateurs de l’immunité (9).
Le délai moyen de diagnostic de la maladie cœliaque est de 12 ans (10). Une étude a par exemple révélé que lorsque la maladie est recherchée de manière active par les médecins généralistes, le taux de diagnostic est alors 32 à 44 fois plus important (11). Cette situation pourrait expliquer en partie le constat selon lequel le nombre de personnes cœliaques aurait été multiplié par 11 entre 1998 et 2007. Nous y reviendrons.
La maladie cœliaque, le caméléon clinique
La maladie cœliaque est ainsi nommée au regard du nombre très important de symptômes non spécifiques. 4 formes différentes de maladie cœliaque sont reconnues en fonction des signes :
- La forme classique : Les signes sont alors ceux attendus en cas de maladie coeliaque, à savoir une malabsorption, des diarrhées, une perte de poids voire un retard de croissance chez l’enfant.
- La forme non classique : les symptômes de malabsorption sont absents, les troubles digestifs ou extra-digestifs sont par contre plus ou moins présents. Dans les deux cas (classique et non classique), les tests sanguins et la biopsie sont anormaux.
- La forme subclinique : l’importance des symptômes est insuffisante pour poser un diagnostic clair. Si un dépistage est toutefois réalisé, les résultats confirment l’existence de la maladie.
- La forme dite potentielle, anciennement qualifiée de maladie cœliaque latente : le test sanguin est alors positif mais la muqueuse intestinale n’est pas (encore) altéré, les signes pouvant toutefois apparaître au cours du temps.
Un test sanguin négatif n’écarte donc pas la maladie cœliaque.
Par ailleurs, une des difficultés potentielles de diagnostic de la maladie cœliaque par biopsie intestinale réside dans le fait qu’un régime sans gluten peut avoir été initié plusieurs semaines avant la réalisation de l’examen. Dans un tel cas, le régime sans gluten « risque » d’être à l’origine de la guérison de l’atrophie des villosités intestinales et donc de révéler un diagnostic… faussement négatif.
Une maladie à part ?
La maladie cœliaque résulte d’un mécanisme caractéristique, à savoir d’une réaction associant une réponse allergique et auto-immune. Elle correspond à une réaction immunitaire en cas de présence de gluten dans l’intestin. Les microvillosités de la muqueuse se retrouvent altérées du fait d’une forte mobilisation de lymphocytes T, de macrophages et de plasmocytes générant une réponse inflammatoire. Le gluten semble le seul composant alimentaire provoquant une telle inflammation intestinale et capable de mobiliser les deux systèmes immunitaires, innés et adaptatifs. Comme évoqué, il existe une prédisposition génétique, notamment via la présence de deux allèles HLA-DQ2. Pour autant, la plupart de la population possède un ou deux de ces allèles sans déclencher la maladie. L’initiation de l’inflammation serait conditionnée à une sensibilisation anormale des lymphocytes CD4+ et la production d’IFN-gamma qui en résulte. Il ne s’agit donc pas d’une maladie auto-immune classique dans la mesure où son déclenchement est totalement dépend de la présence d’un composé étranger, le gluten. Pour autant, des auto-anticorps produits par les lymphocytes B, sont bel et bien mesurés chez tous les patients cœliaques. Ils agissent contre une enzyme-clé sécrétée en cas de consommation de gluten (plus exactement d’un de ses peptides, l’alpha-gliadine), la transglutaminase (tTG). En conclusion, la maladie cœliaque serait due à une action commune des lymphocytes CD4+ et des lymphocytes B, les premiers permettant aux seconds de reconnaitre la transglutaminase.
Que recherche-t-on à travers une prise de sang pour diagnostiquer une maladie cœliaque ?
Il s’agit de tests sanguins (dits sérologiques) mesurant la présence de différents anticorps : anticorps anti-gliadine, anticorps anti-endomysium, anticorps anti-réticuline, anticorps anti-TGt et le dernier né, plus sélectif, les anticorps anti-peptide déamidé de la gliadine (DGP). Le test le plus économique et de référence demeure la recherche d’anticorps anti-TGt de type IgA. Chez les enfants de moins de deux ans, la recherche d’anticorps anti-DGP de types IgA et IgG est toutefois recommandée.
L’analyse du système HLA vous suffirait-il à prédire une maladie cœliaque ?
Malheureusement non. 95% des malades cœliaques sont porteurs des allèles HLA-DQ2 et 5% du HLA-DQ8. 30 % de la population de race blanche possède l’allèle HLA-DQ2 ou HLA-DQ8 mais seulement 4% expriment la maladie17. Si les personnes sont homozygotes pour HLA-DQ2 (les deux gènes contiennent le même allèle), la probabilité grimpe alors à 40%. On parle bien ici de prédisposition, à savoir de la probabilité que, dans un contexte donné (souvent suite à une infection, un stress majeur ou une fatigue importante), votre système immunitaire réagisse contre les certains fragments de peptides du gluten. Vous ne « naissez « pas obligatoirement malade cœliaque.
- Douleurs abdominales ou ballonnements
- Diarrhée chronique
- Distension abdominale
- Maladie hépatique auto-immune
- Thyroïdite auto-immune
- Fatigue chronique
- Altération de l’émail dentaire
- Dermatite herpétiforme
- Trisomie 21
- Parents atteints de maladie cœliaque
- Élévation idiopathique (sans raison connue) des transaminases
- Anémie (de type ferriprive)
- Syndrome du côlon irritable
- Ostéopénie ou ostéoporose
- Neuropathie périphérique
- Stomatite aphteuse récidivante
- Déficit sélectif en IgA
- Perte de poids inexpliquée
- Syndrome de Turner
- Diabète de type 1
- Chez l’enfant : anorexie, constipation chronique, retard de la puberté, retard de croissance, irritabilité, vomissements récurrents, petite taille. Les personnes souffrant de maladie cœliaque voient leurs risques d’être atteints d’autres troubles auto-immuns, notamment de thyroïdite, d’hépatite et de diabète de type 1. Une attention particulière mérite donc d’être menée dans le cadre du suivi médical (13).
2. La dermatite herpétiforme
Il s’agit de la « maladie cœliaque de la peau ». Elle se traduit par l’apparition de petites vésicules cutanées associées à de fortes démangeaisons. Le processus est le même que celui de la maladie cœliaque, à la différence qu’une biopsie de la peau, et non des villosités intestinales, peut suffire à la diagnostiquer. Toutefois une maladie cœliaque est recherchée en parallèle en cas d’apparition de dermatite. 75% des personnes souffrant de cette pathologie présentent une altération de la muqueuse intestinale et 24% une maladie coeliaque44.
3. L’allergie au blé ou l’asthme du boulanger
Comme son nom l’indique, il s’agit ici d’une « allergie », et non d’une atteinte des villosités intestinales comme dans le cas de la maladie cœliaque. Par ailleurs la réponse inadaptée du système immunitaire concerne ici spécifiquement le blé et se traduit par des signes tels que les rougeurs cutanées, des démangeaisons importantes, un visage gonflé (yeux, lèvres, gorge, langue, etc.), des difficultés à avaler, à parler ou à respirer, des troubles digestifs, voire une perturbation du rythme cardiaque (dont l’hypotension) pouvant engendrer une perte de connaissance. Pour autant, cette allergie ne provoque généralement pas de choc anaphylactique (risque mortel).
Cette allergie se réalise par le dosage classique des allergies, à savoir la recherche d’IgE. Elle concernerait entre 0,1 et 0,6% de la population Européenne.
4. L’ataxie au gluten
Il s’agit d’une troisième maladie de type auto-immun en réponse au gluten45. Celle-ci atteint le système neurologique, les anticorps produits à la suite de l’ingestion de gluten attaquent le cervelet, garant de la coordination des mouvements. Étonnamment, il n’existe pas d’atteinte des villosités intestinales, bien que des anticorps anti-transglutaminase 2 sont généralement retrouvés dans l’intestin des personnes souffrant de cette pathologie. L’ataxie au gluten se traduit par une perte d’équilibre, une altération de la parole, de la marche pouvant être à l’origine de chute. L’origine de cette ataxie est encore peu connue, mais certains auto-anticorps semblent s’exprimer davantage dans le cervelet des personnes en souffrant (anticorps anti-transglutaminase tissulaire 6 ou tTG6). A noter que 70% des patients souffrant d’ataxie présentent l’allèle HLA DQ2/B146.
5. L’intolérance aux FODMAP
Késako ? L’argument principal des pro-défenseurs de l’idée selon laquelle tous les maux attribués au gluten ne seraient que pure invention. Plus précisément, il s’agit de l’acronyme anglo-saxon des aliments pouvant être responsables de fermentation par les bactéries de votre microbiote intestinale : « Fermentable Oligosaccharides Disaccharides Monosaccharides And Polyols » ou en français « Polyols, monosaccharides, disacccharides et oligosaccharides fermentescibles ».
A la lecture de la liste (voir tableau du début de l’article), on en arriverait à se demander quels aliments demeurent autorisés… Ce qui fait de ce régime, appelé en toute logique régime FODMAP, un modèle restrictif qui ne doit être réalisé que ponctuellement et dans l’optique de sélectionner de manière personnalisée les aliments tolérés ou non.
On constate que les céréales contenant du gluten (blé, orge, seigle) en font partie. Ils contiennent en effet ce que l’on appelle des fructo-oligo-saccharides (FOS pour les intimes) et plus précisément des fructanes. On parle alors d’intolérance aux fructanes. Plusieurs équipes scientifiques se sont attelées à démontrer que les troubles digestifs dont se plaignent un grand nombre de personnes se déclarant hypersensibles au gluten ne seraient en fait liés « qu’à » la présence de ces glucides fermentescibles. En d’autres termes, leur microbiote se réjouirait un peu trop à recevoir autant de nourriture et les remercierait allégrement par de généreux gaz et ballonnements. Une étude de Février 2018 a par exemple démontré que, dans un groupe de 49 personnes se déclarant hypersensibles au gluten, la consommation de barres de céréales sans gluten, mais contenant des fructanes, engendrait une augmentation des troubles de 15 % en comparaison du même test réalisé avec des barres similaires, elles sans fructanes ni gluten (14). Une étude un peu plus ancienne, publiée dans la revue Gut en 2015 par une équipe australienne a souligné qu’un régime sans FODMAP réduisait le nombre de certaines bactéries intestinales de 47 %, alors qu’un régime qui en était riche favorisait la croissance des bifidobactéries. C’est là toute la difficulté de ce régime.
Il apparaît en effet logique qu’exclure les fructanes, à fortiori chez des personnes souffrant d’une fragilité intestinale, favorise le confort digestif puisqu’il s’agit des aliments responsables de fermentation bactérienne. Cette intolérance concernerait entre 11 et 38% de la population (15). Néanmoins, un tel modèle alimentaire ne peut nullement apparaître optimal pour la santé à long terme du fait des conséquences importantes sur l’équilibre de l’écosystème intestinal. Un régime strict sans aucun FODMAP doit donc être mené de manière ponctuelle (généralement entre 2 et 6 semaines) et instauré avec un professionnel de santé formé, pour permettre de définir une liste personnalisée d’aliments conseillés ou déconseillés. Par ailleurs, les deux situations (intolérance aux fructanes et hypersensibilité au gluten) ne sont pas incompatibles. Même si la suppression des fructanes favorise un certain confort digestif, y compris en présence de gluten, ce n’est pas pour autant qu’une hypersensibilité au gluten ne peut pas exister. En effet, cette dernière n’est pas systématiquement associée à des troubles digestifs et dépend avant tout de l’existence d’une hyperperméabilité intestinale. Ce qui nous amène au point le plus intéressant du sujet de l’article.
Estimation des différents troubles en lien avec la consommation de blé
Comprehensive Reviews in Food Science and Food Safety Vol. 14, 2015
6. L’hypersensibilité non cœliaque au gluten
On parle bien ici d’hypersensibilité et non d’intolérance au gluten. En effet, il est fréquent d’utiliser le second terme, pourtant réservé d’un point de vue sémantique aux glucides (par exemple, l’intolérance au lactose). Le terme d’hypersensibilité désigne une réaction exacerbée de l’organisme contre des fragments de protéines, en l’occurrence ici le gluten.
L’hypersensibilité au gluten se caractérise par l’absence de réponses immunitaires telles que classiquement utilisées pour diagnostiquer les allergies de classe 1 ou la maladie cœliaque. Les villosités intestinales ne sont par ailleurs pas touchées, en sachant toutefois que de nombreuses personnes hypersensibles ne réalisent pas de biopsie villositaire, indispensable mais non suffisante pour confirmer ou infirmer son existence. En clair, vous pouvez souffrir d’une atteinte de votre muqueuse intestinale en tant que personne non-cœliaque, sans le savoir par cet intermédiaire. A noter que d’autres tests permettent de caractériser une hyperperméabilité intestinale associée à une réponse inadaptée au gluten, notamment le dosage de la zonuline voire des LPS (pour lypo-poly-saccharides).
Du fait de cette absence de test positif, de nombreux médecins ou professionnel de santé arguent que cette hypersensibilité est avant tout « dans la tête » de la personne s’en plaignant ou un vulgaire phénomène de mode dont profitent certains industriels, ou dans le meilleur des cas secondaire à l’intolérance aux FODMAP. C’est là tout le danger de la médiatisation à outrance couplée à la recherche d’un coupable universel de tous les maux de la société. Certes, il existe à mon sens une partie de la population prônant une alimentation stricte sans gluten (pensant agir positivement pour leur santé) qui pourrait tout à fait s’autoriser une consommation modérée de gluten. Pour autant, évoquer que toute la population voyant ses troubles intestinaux s’améliorer après avoir réduit ou supprimer le gluten de son alimentation, n’est sujette qu’à l’effet placebo ou des FODMAP, s’avère quelque peu… rigide.
La littérature scientifique (au-delà de la preuve par l’expérience) s’étoffe. La proportion de personnes souffrant de cette hypersensibilité au gluten (ce que l’on nomme la prévalence en jargon scientifique) est aujourd’hui évaluée entre 0,5% pour les plus pessimistes et 13% pour les autres (voire 35% pour certains auteurs). L’étau statistique se resserre donc, même s’il demeure encore imprécis (16). En revanche, de manière très pratique, l’existence de nombre des symptômes liés à cette hypersensibilité peut permettre de préciser l’intérêt de réduire, voire de supprimer le gluten. On peut citer par exemple les douleurs abdominales, des brûlures épigastriques, de la rétention d’eau, des nausées, des diarrhées, des constipations ou une alternance, des maux de tête, une fatigue, des troubles immunitaires (susceptibilité aux infections, allergies, hypersensibilité à d’autres aliments ou composés non alimentaires, pathologies auto-immunes), des troubles inflammatoires (troubles en -ite, en particulier au niveau ostéo-articulaire ou des microcapillaires), voire du comportement (autisme, troubles de l’attention avec ou sans hyperactivité).
Il est toutefois essentiel de bien comprendre que l’hypersensibilité au gluten n’est pas seule en cause en cas de manifestation de ces symptômes. Ils peuvent en effet se manifester de manière différente en fonction de :
- L’existence d’une hyperperméabilité intestinale, à l’origine d’un passage important de peptides alimentaires (ou bactériens) comme le gluten et pouvant engendrer une réponse inadaptée de votre système immunitaire.
- La qualité de votre microbiote intestinal. Les bactéries présentes dans votre intestin modulent en effet votre réponse immunitaire.
- Votre prédisposition génétique. En fonction de la nature de votre système HLA (HLA-DQ2 et HLA-DQ8 dans le cas de la maladie cœliaque comme évoqué précédemment et HLA DQ-DR pour l’hypersensibilité au gluten), la probabilité que vos cellules immunitaires réagissent contre les protéines de gluten varie de manière très importante. La nature de votre système HLA permet d’ailleurs d’expliquer en partie la variabilité des réactions selon les personnes.
L’écosystème intestinal au cœur du sujet
Jusqu’au début des années 2000, l’intestin était considéré comme un vulgaire tuyau, destiné à assimiler les nutriments et à faciliter le transit. Aujourd’hui, il est au cœur des actualités scientifiques les plus récentes. Nous sommes en effet dans une nouvelle étape décisive, passionnante, de découvertes des liens étroits pouvant exister entre l’écosystème intestinal et la préservation de la santé. Diabète, obésité, troubles métaboliques, troubles du comportement, autisme, hyperactivité, Alzheimer, Parkinson, sclérose en plaques, polyarthrite rhumatoïde, maladie de Cröhn, rectocolite hémorragique, etc. Autant de pathologies dont on a démontré les liens avec une perturbation de l’écosystème intestinal. Car on parle bien ici d’écosystème et non pas simplement d’intestin ou de microbiote, nouveau terme désignant les bactéries de la flore présente dans votre intestin.
Cet écosystème repose sur un trépied interdépendant :
- Votre microbiote est constitué d’environ 100 000 milliards de bactéries. Il pèse plus d’1,5 kg, contient 10 fois plus de bactéries que vous n’êtes constitué de cellules et une information génétique 150 fois plus importante ! Bien entendu, ce microbiote interagit avec vous en permanence.
- Votre muqueuse intestinale, représente environ 300 m2 de surface, soit davantage qu’un terrain de tennis. Elle est constituée de cellules (les entérocytes) organisées en microvillosités dont le rôle principal est d’assimiler les nutriments issus de vos aliments, tout en empêchant le passage important de peptides alimentaires ou bactériens issus de la lumière intestinale (le tube de l’intestin) comme le gluten qui nous intéresse ici.
- Votre système immunitaire : 70% de celui-ci est en lien avec les deux autres éléments de votre trépied, la muqueuse intestinale et le microbiote. Cette interaction lui permet d’acquérir les propriétés indispensables pour vous permettre de vous défendre des infections, tout en tolérant les peptides issus de votre alimentation ou de l’environnement et ainsi de réduire les risques de survenue d’intolérances ou d’allergies.
Le déséquilibre de cet écosystème intestinal peut avoir de nombreuses origines :
- L’implantation de certaines bactéries potentiellement pathogènes ou de champignons tel que le Candida Albicans (à l’origine de la Candidose).
- La baisse de diversité bactérienne, à la suite par exemple d’une naissance par césarienne, à une prise d’antibiothérapie, une alimentation riche en graisses saturées ou en sucres, un manque de fibres (point clé d’une santé optimale), une consommation accrue d’édulcorants (17), de perturbateurs endocriniens comme le Bisphénol A (18, 19), d’additifs tels que le dioxyde de titane omniprésent dans l’alimentation, la sédentarité (20), le stress chronique, etc.
- L’inflammation de la muqueuse intestinale, pouvant être liée à une surexposition à certains peptides alimentaires comme le gluten ou les caséines laitières, la baisse de diversité bactérienne que l’on vient d’évoquer, une activité physique intense, une surconsommation de protéines, un défaut de mastication, un déficit nutritionnel (en Glutamine, vitamine D, antioxydants, Zinc ou vitamine A notamment), le recours à une supplémentation mal assimilée comme le Fer par exemple.
Cette inflammation de la muqueuse va se traduire par un passage anormal et important de peptides alimentaires ou bactériens, notamment ce que l’on nomme les LPS (Lypo-Poly-Saccharides) à l’origine de réactions immunitaires ou inflammatoires chez des personnes dont le système immunitaire est prédisposé. On parle alors d’hyperperméabilité intestinale (ou HPI) ou de Leaky Gut Syndrom. De manière illustrée, votre intestin devient alors une passoire.
A noter que votre microbiote intestinal s’installe dès le plus jeune âge, au cours des premiers mois de vie, voire vraisemblablement dès la vie intra-utérine (21). Un accouchement par voie naturelle, l’allaitement, une alimentation pauvre en protéines, l’absence d’antibiothérapie chez le nourrisson sont par exemple autant de facteurs favorisant une implantation bactérienne saine et variée, notamment en bifidobactéries bénéfiques pour la santé. Ce microbiote aura alors tendance à revenir à sa composition initiale tout au long de la vie, même si des variations peuvent intervenir du fait des éléments évoqués ci-dessus. En bref, l’implantation du microbiote au cours de la première année de vie est particulièrement importante.
Une nuance mérite toutefois d’être développée concernant le premier point évoqué, à savoir la nécessité de l’existence préalable d’une hyperperméabilité intestinale. En effet, le gluten présente la spécificité de stimuler une protéine particulière – la zonuline – présente à la surface de la muqueuse intestinale et régulant les échanges osmolaires entre la lumière de l’intestin et le milieu intérieur. L’activation importante et prolongée de zonuline a pendant longtemps été considérée comme spécifique de la maladie cœliaque. Or plusieurs études ont montré que cette production était bel et bien présente également chez les personnes se plaignant d’hypersensibilité au gluten. Elle s’avère dans ces conditions moindre et plus ponctuelle (22,23). Le gluten pourrait donc être considérée autant comme la cause que la conséquence de troubles digestifs, voire de réponses immunitaires inadaptées.
La notion d’hypersensibilité au gluten est donc aujourd’hui établie (16, 24). D’autres mécanismes ont mis en évidence l’existence, chez les personnes se plaignant d’hypersensibilité au gluten, d’une modulation immunitaire par certains messagers (les chimiokines de type CXL10 et les LPS) (25) et d’une hyperperméabilité intestinale (26). Toute la difficulté demeure de quantifier la proportion de personnes concernées et de distinguer cette hypersensibilité de l’intolérance aux fructanes.
Enfin, l’expression d’hypersensibilité au gluten est couramment utilisée, je l’indique d’ailleurs ainsi dans l’article, afin de simplifier le sujet. La fraction du gluten concernée est en réalité la glyadine et, de manière encore plus précise, la teneur en un fragment spécifique, le peptide 33-mer (27). Les effets possibles du gluten ont par ailleurs été distingués en fonction de la nature des peptides contenus dans cette protéine (le peptide 31 à 43 serait cytotoxique, le peptide 57 à 89 modulerait la réponse immunitaire, les peptides 111 à 130 et 151 à 170 libéreraient la zonuline et les peptides 261 à 277 induiraient la libération de cytokines pro-inflammatoires) (4) .
Références :
- https://www.sante-et-nutrition.com/gluten-diabete/
- https://www.sciencesetavenir.fr/sante/coeur-et-cardio/les-regimes-sans-gluten-ne-sont-pas-benefiques-contre-les-maladies-cardiovasculaires_112669
- Benjamin Lebwohl et al., Long term gluten consumption in adults without celiac disease and risk of coronary heart disease: prospective cohort study BMJ 2017; 357 doi: 10.1136/bmj.j1892.
- Elma MJ Salentijn et al., Celiac disease T-cell epitopes from gamma-gliadins : immunoreactivity depends on the genome of origin, transcript frequency, and flanking protein variation BMC Genomics. 2012; 13: 277. doi: 10.1186/1471-2164-13-277
- Rubio-Tapia A et al, Increased prevalence and mortality in undiagnosed celiac disease. Gastroenterology. 2009 Jul;137(1):88-93. doi: 10.1053/j.gastro.2009.03.059.
- Paola Migliorini et al, Agronomic and quality characteristics of old, modern and mixture wheat varieties and landraces for organic bread chain in diverse environments of northern Italy European Journal of Agronomy Volume 79, September 2016. doi : 10.1016/j.eja.2016.05.011.
- Alessio Fasano et al., Prevalence of Celiac Disease in At-Risk and Not-At-Risk Groups in the United States A Large Multicenter Study Original Investigation February 10, 2003 Arch Intern Med. 2003;163(3):286-292. doi:10.1001/archinte.163.3.286.
- Rubio-Tapia A et al., ACG clinical guidelines: diagnosis and management of celiac disease. Am J Gastroenterol. 2013 May;108(5):656-76; quiz 677. doi: 10.1038/ajg.2013.79.
- Mohsin Rashid et al., Tests sérologiques dans la maladie cœliaque. Guide pratique à l’usage des cliniciens Can Fam Physician. 2016 Jan; 62(1): e11–e17.
- Pulido O et al., Clinical features and symptom recovery on a gluten-free diet in Canadian adults with celiac disease. Can J Gastroenterol. 2013 Aug;27(8):449-53.
- Catassi C et al., Detection of Celiac disease in primary care: a multicenter case-finding study in North America. Am J Gastroenterol. 2007 Jul;102(7):1454-60.
- Rostom A et al., American Gastroenterological Association (AGA) Institute technical review on the diagnosis and management of celiac disease. Gastroenterology. 2006;131(6):1981–2002.
- Kelly CP et al., Advances in diagnosis and management of celiac disease. Gastroenterology. 2015;148(6):1175–86).
- Skodje GI et al., Fructan, Rather Than Gluten, Induces Symptoms in Patients With Self-Reported Non-Celiac Gluten Sensitivity. Gastroenterology. 2018 Feb;154(3):529-539.e2. doi: 10.1053/j.gastro.2017.10.040.
- Manfred Kroger, Comprehensive Reviews in Food Science and Food. Impact Factor: 5.974. ISI Journal Citation Reports.
- Elli L et al., Diagnosis of gluten related disorders: Celiac disease, wheat allergy and non-celiac gluten sensitivity. World J Gastroenterol. 2015 Jun 21;21(23):7110-9. doi: 10.3748/wjg.v21.i23.7110.
- Suez J et al., Artificial sweeteners induce glucose intolerance by altering the gut microbiota. Nature. 2014 Oct 9;514(7521):181-6. doi: 10.1038/nature13793. Epub 2014 Sep 17.
- Lai KP et al., Bisphenol A alters gut microbiome : Comparative metagenomics analysis. Environ Pollut . 2016 Nov.
- Zhongyuan Guo et al., Titanium dioxide nanoparticle ingestion alters nutrient absorption in an in vitro model of the small intestine. NanoImpact, 2017; 5: 70
- Allen JM et al., Exercise Alters Gut Microbiota Composition and Function in Lean and Obese Humans. Med Sci Sports Exerc. 2017 Nov 20. doi: 10.1249/MSS.0000000000001495.
- JP Langhendries et al., Acquisition de la flore intestinale néonatale: rôle sur la morbidité et perspectives thérapeutiques. Archives de Pédiatrie. Volume 5, Issue 6, June 1998 , Pages 644-653 https://doi.org/10.1016/S0929-693X(98)80172-3.
- Fasano. 2011 « Zonulin and Its Regulation of Intestinal Barrier Function: The Biological Door to Inflammation, Autoimmunity, and Cancer ». Physiological Reviews 151-175.
- Hollon et al. 2015. “Effect of gliadin on permeability of intestinal biopsy explants from celiac disease patients and patients with non-celiac gluten sensitivity”. Nutrients 7(3):1565-1576
- Fasano A, Catassi C. Clinical practice. Celiac disease. N Engl J Med. 2012;367(25):2419–26.
- Melanie Uhde et al., Intestinal cell damage and systemic immune activation in individuals reporting sensitivity to wheat in the absence of coeliac disease Gut. 2016 Dec; 65(12): 1930–1937. Published online 2016 Jul 26. doi: 10.1136/gutjnl-2016-311964.
- Hollon et al. 2015. “Effect of gliadin on permeability of intestinal biopsy explants from celiac disease patients and patients with non-celiac gluten sensitivity”. Nutrients 7(3):1565-1577.
- Lacaze X. et al., (2014). Implication de différentes classes de gliadines du blé dur dans la maladie coeliaque. Mise en évidence par analyses RP-HPLC et ELISA dans une collection de blés durs. Industries des Céréales, 187, 15-17. https://prodinra.inra.fr/record/263175.







Article très intéressant surtout pour toutes ces personnes qui ont le syndrome de l’intestin irritable et qui touche surtout les femmes .. C’est pas facile au quotidien.
Merci pour toutes ces informations
Bonne continuation
Sandra M
M’avoir fait subir la biopsie du duodenum après 6 mois d’arrêt du gluten pour me proposer que me soient remboursés des produits sans gluten bien inutils… une honte du système médical!
Résultat bien sûr… « vous pouvez manger du gluten », mais au bout de quelques jours je savais bien quel test était le bon!
Article très complet merci. Il est vrai que le gluten on peut largement s’en passer. J’ai même une amie qui a perdu 5 kg en 2 semaines en ayant seulement arrêté le gluten.
Contenu passionnant. Merci pour ce partage ! Je déplore cependant que le sujet ne soit pas assez maîtrisé par la plupart des médecins traditionnels conduisant à de coûteux examens souvent inutiles et l‘absence de diagnostic. J‘ai dû ainsi moi-même me pencher sur le problème après avoir consulté moult médecins…
Merci pour cet article passionnant. Il m’aide à mieux comprendre les maux dont je souffre. Mon état de santé s’est nettement amélioré avec un régime strict depuis 5 ans. Je découvre l’existence de la dermatite herpétiforme. Je souffre de poussées de ce que l’on pense être du « psoriasis en goutte » associées à des réactions immunitaires. Je suis convaincue de l’importance du microbiote pour apaiser mon sytème immunitaire, mais je ne trouve personne pour m’aider dans cette voie. Je suis preneuse de tous vos conseils!!
Bonjour Anne-Valérie,
Dans quelle région êtes-vous ? Je peux tenter de vous orienter vers quelqu’un en fonction.
Bonjour, je recherche un professionnel qui pourrait m’aiguiller dans le diagnostic ; je note quelques symptômes inflammations (-ite) articulaires depuis de nombreuses années, important retard croissance pendant enfance, fatigue chronique, suspicion dermatite herpétiforme (je vais allez voir ma dermato), altération émail dentaire… Mais qui allait voir ? Je suis sur Toulouse…
Comment rééquilibre son microbiote intestinal
Merci pour ce superbe article, cela fait plaisir! Je suis d’accord avec vous et je fais faire les mêmes tests sur 5 semaines. Les diagnostics de maladie coeliaque ne sont souvent pas fiables pour de multiples raisons (cf. Alessio Fasano) et il est important de toujours prendre au sérieux les symptômes.
J’ai trouvé votre article par hasard, et c’est intéressant .
Bonjour
Je vous remercie pour cet article très complet concernant le gluten, mais qui me semble contenir de grosses lacunes, et qui devraient, je crois, être tenus en compte, et celà concerne le côté matière première de la farine et l’ascpect suivant: la confection des pâtes en boulangerie.
En effet, probablement 90% des meuniers rajoutent dans leurs farines –
-du gluten (après séparation industrielle du gluten et de l’amidon
-souvent du lactose et du soja
De façon à obtenir des farines facilement panifiables et surtout très régulières
Au niveau des boulangers eux même, très peut savent encore travailler des farines natives
(sans aucun rajout d’additifs d’aide à la panification: dans les écoles de boulangerie, ces produits souvent chimiques sont prônés auprès des élèves: voir catalogue de « puratos ».
Je ne vois pas plus évoquer le fait que beaucoup de boulangers rajoutent de la matière grasse à leur pâte, tant végétale que animale (cela empêchera le gluten de se gorger d’eau et de se dénaturer par l’action des levures et de enzymes présents dans la pâte)
De plus, les températures de pâtes, aux alentour de 25° ,accélère le processus de levée de ces même pâtes (de même que tous les « améliorants » utilisés) qui empêche également le gluten d’avoir le temps de se gorger d’eau.
Voilà quelque commentaires qui méritent peut-être de se poser d’autres questions sur les processus de fabrication actuelle des pains qui contiennent du gluten pas si mauvais que ça s’il est bien travaillé.
Bien à vous
Pascal Donnet
Bonjour.
Merci pour ce long et passionnant article.
Je découvre beaucoup de choses…
Êtes vous en mesure de conseiller un ou deux praticiens sensibilisés à ces sujet, dans la région de Montpellier ?..
Je vous remercie. Je ne connais malheureusement personne à vous conseiller dans ce secteur.
Où avez-vous trouvé des fructanes dans les céréales ?
Le polysaccharide majeur des graines de céréales est l’amidon (il représente 80% des constituants du grain, lui même composé de chaines d’amylose et d’amylopectine. Puis 15 % de protéines, 2% de lipides, 2% de pentosanes, 1 % pour tout le reste, fibres/sons (cellulose), minéraux…
Bonjour,
Je voudrai savoir si vous connaissez quelqu’un sur Lille. Je suis dans l’incompréhension la plus totale sur mes symptômes.